Энтальпия воздуха
Понятие энтальпии можно объяснить как потенциал, который может совершить работу. Чем больше энтальпия, тем большую работу сможет совершить вещество при воздействии на него. Предположим нужно сжать воздух таким образом, чтобы он нагрелся до определённой температуры, возьмём 50°C. Так вот, для того, чтобы до этой температуры нагрелся воздух с меньшей энтальпией, его нужно сжать сильнее, чем воздух с большей энтальпией.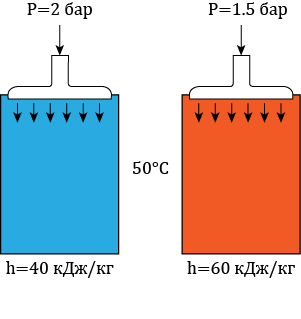
Воздух состоит из двух частей - сухой части (собственно воздух) и скрытая в воздухе влага (вода). В системах кондиционирования для расчётов используются параметры этой смеси влажного воздуха и воды (то есть влажный воздух), и энтальпия такого воздуха складывается из энтальпий двух его частей, упомянутых выше: $$h=h_{da}+d \cdot h_{g}$$
Энтальпия сухого воздуха: $$h_{da} \approx 1.004 \cdot t$$ Энтальпия насыщенного водяного пара: $$h_g \approx 2500+1.86 \cdot t$$ Энтальпия влажного воздуха: $$h \approx 1.004 \cdot t + d \cdot (2500+1.86 \cdot t)$$ Температура: $$t=\frac{h-2500\cdot d}{1.004+1.86\cdot d}$$ Влагосодержание: $$d=\frac{h-1.004\cdot t}{2500+1.86\cdot t}$$
\(h\) - энтальпия влажного воздуха, кДж/кг
\(h_{da}\) - энтальпия сухого воздуха, кДж/кг
\(d\) - влагосодержание, кг (вода)/кг (сухой воздух)
\(h_g\) - энтальпия насыщенного водяного пара, кДж/кг
Источники
[1] ISBN 5-89565-005-8
С.И.Бурцев, Ю.Н.Цветков - Влажный воздух. Состав и свойства (формула 4.28)